 ""
""
近日,复宏汉霖发布了2025年年报,公司实现营业收入66.67亿元,同比增长16.5%;实现归母净利润8.27亿元,同比增长0.80%。
作为业内少有的跑通研发、临床、生产、商业化的盈利Biopharma(生物制药公司),复宏汉霖面临着创新转型的课题:2022年3月,公司首款创新药获批,却已是国内第7款上市的国产PD-1单抗,该赛道被贴上“内卷”标签;“中国生物类似药之王”的称号曾为其筑起业绩基本盘,却也在集采浪潮下成为公司转型的压力。
公司的创新含量有多高?“箭在弦上”的生物药集采对公司业绩的冲击有多大?2026年亚布力中国企业家论坛年会期间,复宏汉霖执行董事、首席执行官朱俊在接受《每日经济新闻》记者专访时回应了这些问题。
朱俊认为,生物类似药的技术壁垒被低估,“创新药可以‘画大饼’,但生物类似药并非所有公司都有能力做”。他同时坦言,一家伟大的药企绝不能依赖规模堆砌收入,而是要打造一款人尽皆知的“大药”,这是复宏汉霖的转型目标。
未来两年开始,降低成熟产品在中国的预期2025年,复宏汉霖的产品总收入约57.75亿元,同比增长17.0%。其中,HER2单抗药物曲妥珠单抗(商品名:汉曲优)仍是公司的现金牛产品,在国内的收入同比增长4.3%,达到28.09亿元,其在欧盟、美国获批的同款产品Zercepac和Hercessi销售合计1.55亿元。
收入占比第二的是PD-1单抗药物斯鲁利单抗(商品名:汉斯状),去年其收入同比增长10.0%,达到14.40亿元;其在欧盟、印尼获批的同款产品Hetronifly、Zerpidio实现销售收入约5280万元。
再加上其他获批产品,生物类似药撑起了复宏汉霖近七成产品收入。但随着去年11月部分生物类似药被纳入第十批国家药品集中采购范围,最高降价幅度达到90%,市场对复宏汉霖的业绩预期有些担忧。
对此,朱俊认为市场变化是行业常态,公司更关注如何通过创新和出海打开新空间。
首先是汉斯状用于胃癌围手术期治疗的适应证有望于2026年获批,这是全球首个胃癌围手术期以免疫单药取代术后辅助化疗的治疗方案,预计将给公司带来50%以上的国内收入增长。
第二,随着汉斯状、帕妥珠单抗(HLX11)分别在欧盟、美国获批,海外的收入增长会成为公司业绩的重要支撑——值得一提的是,HLX11是美国首款且唯一获批的帕妥珠单抗生物类似药。
朱俊说,公司会弱化生物类似药在中国市场的预期,“2027年、2028年开始,我就不再关注国内生物类似药的收入数据了”。
海外收入突破2亿元,欧美市场将于今年放量增长正如朱俊所说,复宏汉霖去年在海外市场动作频频,迎来BD(商务拓展)交易爆发年,仅2025年上半年,公司合同现金流入超10亿元,同比增长280%。
从产品落地来看,汉曲优已在全球50多个国家和地区获批上市,在海外的合作伙伴多达6家;汉斯状也在全球40多个国家和地区获批上市。公司海外产品去年整体收入首次超过2亿元,占总营收的比重约3%。
-1775037196346_transcode.jpg)
2025年主要产品收入构成(单位:亿元)
差异化创新何时兑现?
目前,中国创新药行业进入高质量发展阶段,BD交易成为全球市场核心驱动力。据国盛证券统计,2025年中国相关交易总金额提升至1388亿美元,同比增加135%,占全球交易总金额约50%。随着“创新药+国际化”双轮驱动商业模式跑通,多家创新药企业在2025年实现扭亏为盈,行业已从“烧钱研发”进入“盈利兑现”新阶段。
在此背景下,朱俊觉得复宏汉霖还有很多事情要做。“靠一个个小资产搭起来的收入,哪怕年收入1000亿美元,这个公司也不伟大,你是靠量堆出来的;如果说这个公司就做了一个产品,每个人都知道这个产品的名字,这才是伟大,我们希望做后者。”
过去几年,复宏汉霖着手搭建创新管线。从最新公布的临床前管线的数量和创新性看,公司明显加大了对BIC(同类最优)和FIC(同类首个)资产的布局。与此同时,公司去年确认研发开支约24.92亿元,同比增长35.39%,是4年前的2倍。
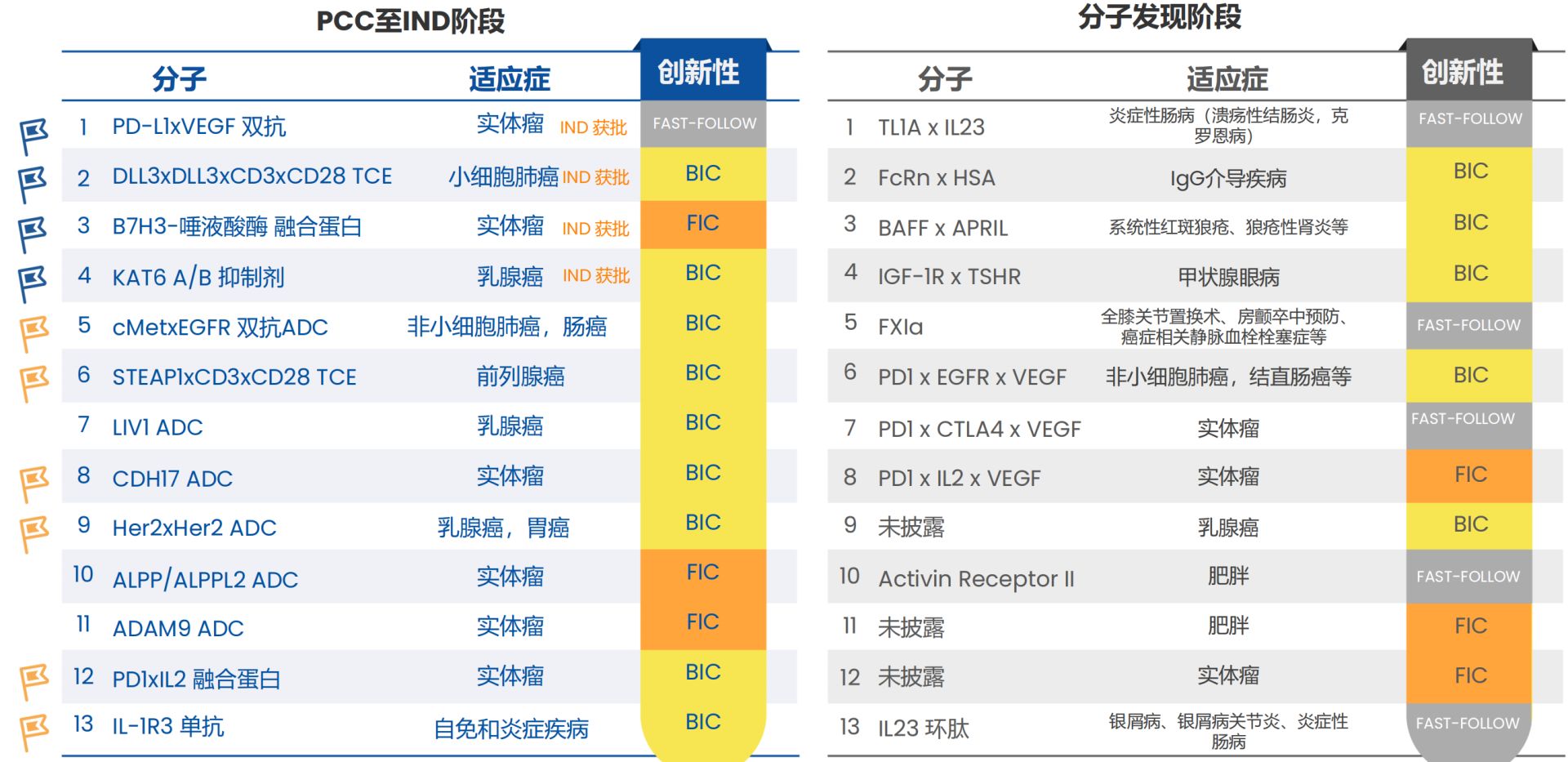
临床前产品管线
ADC药物HLX43、EGFR单抗HLX07。值得注意的是,与公司此前布局生物类似药的思路一致,公司在热门赛道里寻觅差异化靶点或者适应证。
在朱俊的构想里,今年有望拿下“胃癌围手术期治疗”适应证的PD-1抑制剂,是最有可能实现年收入跃升的创新药,甚至有可能在国产创新药的年销售额排名中拿个好名次。
但该品种的商业化仍面临现实挑战。此前,PD-1赛道经历估值跳水,叠加后续医保谈判的降价压力,汉斯状新适应证的商业化前景仍有变数,投资者普遍持谨慎态度,对BD行情火爆的ADC赛道兴趣更高——今年1月,公司在美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)上首次公布HLX43治疗复发/转移性食管鳞癌(ESCC)的II期概念验证(POC)数据后,公司股价大涨。
目前,HLX43已布局非小细胞肺癌、宫颈癌、食管鳞癌、胸腺癌等多个实体瘤适应证,其中,肺癌领域研发进展最快,公司计划于今年第四季度启动该药物针对二线EGFR野生型非鳞状非小细胞肺癌、三线及以上鳞状非小细胞肺癌的注册性临床。不过,即便研发进展顺利,按照理想预期,这款药物距离在国内获批上市仍有约3年时间。